INOCA/ANOCA problem, który dotyka około 1.5-2 mln pacjentów w Polsce [wywiad]
Opublikowane: 13 czerwca 2025 Filed under: Choroby, Ogólne, Układ krążenia | Tags: ból w klatce piersiowej, diagnostyka, dysfunkcja mikrokrążenia, dławica, kardiologia, leczenie, niedokrwienie, świadomy pacjent Dodaj komentarz
Większość pacjentów z INOCA/ANOCA nie jest skutecznie leczona, mimo dostępności tanich i skutecznych leków. Warto byśmy wspólnie to zmienili – warto wiedzieć czym jest INOCA/ANOCA i jak diagnozować ten zespół chorobowy.
O tym czym jest zespół INOCA/ANOCA, jak rozpoznać i leczyć rozmawiałem w wywiadzie na zaproszenie redaktor Marty Sułkowskiej (przeczytaj pełen wywiad).
Analiza blaszki miażdżycowej: przełom we wczesym wykrywaniu miażdżycy tętnic wieńcowych.
Opublikowane: 11 Maj 2025 Filed under: AI, Prewencja, Układ krążenia | Tags: AI, artificial-intelligence, atherosclerosis, blaszka miażdżycowa, cad, cardiology, CCTA, coronary, coronary-angiogram, heart-attack, kardiologia, koronarografia, Nowe Technologie, Prewencja, sztuczna inteligencja, technology, tomografia komputerowa, zawał, świadomy pacjent Dodaj komentarzPowszechnie nazywana „wieńcówką”, a fachowo jest to „zespół wieńcowy” – choroba polegająca na odkładaniu się złogów cholesterolu w ścianach tętnic wieńcowych, prowadząca do niedokrwienia mięśnia sercowego i zawału serca. Rozwija się latami, a pierwsze zmiany w ścianach tętnic obecne są już u 20. czy 30-latków – jednak na tym etapie nie dają żadnych objawów.

źródło: Nieman K et al J Cardiovasc Comput Tomogr. 2024 Sep-Oct;18(5):429-443.
Pierwsze dolegliwości pacjenci zaczynają czuć dopiero po 50. roku życia w postaci ucisku w klatce piersiowej, uczucia zatykania czy krótkiego oddechu związanego z wysiłkiem. Niestety pierwszym klinicznym objawem może też być zawał serca – bez jakichkolwiek objawów przepowiadających. Nic więc dziwnego, że pojawia się pytanie, czy jesteśmy w stanie wykryć miażdżycę tt. wieńcowych na wczesnym etapie i określić, jak bardzo jest zaawansowana, a w razie potrzeby zahamować?
Złotym standardem oceny tętnic wieńcowych jest koronarografia – inwazyjne badanie polegające na wprowadzeniu cewnika do naczynia wieńcowego i nagraniu, jak podawany przez niego kontrast wypełnia światło naczynia, w celu wykrycia zwężeń. Nie jest to jednak metoda, którą można by stosować powszechnie w formie skriningu populacji. Od blisko dekady obserwujemy dynamiczny rozwój tomografii komputerowej tętnic wieńcowych, coraz częściej nazywanej „nieinwazyjną koronarografią”, polegającej na wykonaniu skanu tętnic wieńcowych w czasie kilku sekund, bez konieczności wprowadzania cewników do aorty.
Poza standardową analizą obrazów obejmującą ocenę światła tętnic wieńcowych, możliwa jest również ocena budowy ściany naczyń, a w szczególności skwantyfikowania blaszek miażdżycowych, a tym samym wykrycia choroby na bardzo wczesnym etapie. Dotychczas takie analizy były dostępne w zasadzie wyłącznie w ramach projektów akademickich, gdyż były wykonywane manualnie, co zajmowało do kilkunastu godzin na przypadek. Wraz z upowszechnieniem metod obliczeniowych opartych na sztucznej inteligencji, proces ten został znacznie przyspieszony, co pozwoliło na udostępnienie metody szerszej populacji pacjentów.
W ramach analizy blaszki miażdżycowej (ang. plaque analysis) otrzymujemy nie tylko informację o jej objętości (ang. Total Plaque Volume), ale także o podziale na podstawowe podtypy (blaszka uwapniona, nieuwapniona, o niskiej atenuacji), a to pozwala określić jakie jest ryzyko jej pęknięcia (zawału serca), a także potencjalną odpowiedź na leczenie farmakologiczne. Ponadto wykonanie kontrolnego badania po określonym leczeniu pozwala na weryfikację, czy obserwowana miażdżyca nasiliła się, uległa stabilizacji, a może udało się ją częściowo cofnąć.
Poniżej kilka przykładów technologii do oceny blaszki miażdżycowej dostępnych do zastosowania klinicznego. Wydaje się, że w najbliższej dekadzie takie podejście ma szansę stać się metodą skriningu pacjentów w kierunku miażdżycy, zanim pojawią się objawy.



Dostępność zaawansowanej oceny blaszek miażdżycywych nadal pozostaje ograniczona. Mimo, że powyższe analizy są objęte refundacją choćby w Stanach Zjednoczonych, to ich użycie w naszej szerokości geograficznej dostępne jest wyłącznie komercyjnie. Tymniemniej, śledząc postęp i wyniki kolejnych badań naukowych należy się spodziewać, że wdrożenie analizy balszki miażdżycowej w oparciu o tomografię komputerową tętnic wieńcowych jako elementu prewencji pierwotnej zawałów serca jest kwestią czasu.
Referencje:
- Nieman K, García-García HM, Hideo-Kajita A, Collet C, Dey D, Pugliese F, Weissman G, Tijssen JGP, Leipsic J, Opolski MP, Ferencik M, Lu MT, Williams MC, Bruining N, Blanco PJ, Maurovich-Horvat P, Achenbach S. Standards for quantitative assessments by coronary computed tomography angiography (CCTA): An expert consensus document of the society of cardiovascular computed tomography (SCCT). J Cardiovasc Comput Tomogr. 2024 Sep-Oct;18(5):429-443. doi: 10.1016/j.jcct.2024.05.232. Epub 2024 Jun 6. PMID: 38849237.
- Bär S, Knuuti J, Saraste A, Klén R, Kero T, Nabeta T, Bax JJ, Danad I, Nurmohamed NS, Jukema RA, Knaapen P, Maaniitty T. Derivation and Validation of an Artificial Intelligence-Based Plaque Burden Safety Cut-Off for Long-Term Acute Coronary Syndrome from Coronary Computed Tomography Angiography. Eur Heart J Cardiovasc Imaging. 2025 Apr 17:jeaf121. doi: 10.1093/ehjci/jeaf121. Epub ahead of print. PMID: 40243706.
- Dahdal J, Jukema RA, Maaniitty T, Nurmohamed NS, Raijmakers PG, Hoek R, Driessen RS, Twisk JWR, Bär S, Planken RN, van Royen N, Nijveldt R, Bax JJ, Saraste A, van Rosendael AR, Knaapen P, Knuuti J, Danad I. CCTA-Derived Coronary Plaque Burden Offers Enhanced Prognostic Value Over CAC Scoring In Suspected CAD Patients. Eur Heart J Cardiovasc Imaging. 2025 Mar 25:jeaf093. doi: 10.1093/ehjci/jeaf093. Epub ahead of print. PMID: 40131307.
- Kim DH, Kim SH, Chu HW, Kang SH, Yoon CH, Youn TJ, Chae IH. Validation of artificial intelligence-based quantitative coronary angiography. Digit Health. 2024 Dec 18;10:20552076241306937. doi: 10.1177/20552076241306937. PMID: 39698508; PMCID: PMC11653446.
- Tzimas G, Gulsin GS, Everett RJ, Akodad M, Meier D, Sewnarain K, Ally Z, Alnamasy R, Ng N, Mullen S, Rotzinger D, Sathananthan J, Sellers SL, Blanke P, Leipsic JA. Age- and Sex-Specific Nomographic CT Quantitative Plaque Data From a Large International Cohort. JACC Cardiovasc Imaging. 2024 Feb;17(2):165-175. doi: 10.1016/j.jcmg.2023.05.011. Epub 2023 Jul 5. PMID: 37410009.
- Chan K, Wahome E, Tsiachristas A, Antonopoulos AS, Patel P, Lyasheva M, Kingham L, West H, Oikonomou EK, Volpe L, Mavrogiannis MC, Nicol E, Mittal TK, Halborg T, Kotronias RA, Adlam D, Modi B, Rodrigues J, Screaton N, Kardos A, Greenwood JP, Sabharwal N, De Maria GL, Munir S, McAlindon E, Sohan Y, Tomlins P, Siddique M, Kelion A, Shirodaria C, Pugliese F, Petersen SE, Blankstein R, Desai M, Gersh BJ, Achenbach S, Libby P, Neubauer S, Channon KM, Deanfield J, Antoniades C; ORFAN Consortium. Inflammatory risk and cardiovascular events in patients without obstructive coronary artery disease: the ORFAN multicentre, longitudinal cohort study. Lancet. 2024 Jun 15;403(10444):2606-2618. doi: 10.1016/S0140-6736(24)00596-8. Epub 2024 May 29. PMID: 38823406; PMCID: PMC11664027.
Kiedy zacząć dbać o serce?
Opublikowane: 19 kwietnia 2024 Filed under: Choroby, Prewencja, Układ krążenia | Tags: badania profilaktyczne, cholesterol, kardiologia, serca Dodaj komentarz
Wyniki badania Apple Heart Study
Opublikowane: 23 sierpnia 2019 Filed under: Badania kliniczne, Układ krążenia Dodaj komentarzZnamy wyniki badania Apple Heart Study przeprowadzonego przez badaczy uniwersytetu Standford. Wywiad ze współbadaczem dr. Mintu Turakhia.
Smartfon w diagnostyce i leczeniu chorób przewlekłych.
Opublikowane: 27 stycznia 2019 Filed under: AI, Choroby, Układ krążenia, Układ oddechowy | Tags: dla pacjenta, ekg, mHealth, Nowe Technologie, Prywatna Praktyka, self-monitoring, smartfon, telemedycyna Dodaj komentarzKiedy jeszcze smartfon może pomóc w diagnostyce i leczeniu? Jak sprawdza się nowoczesne #EKG? Czy sztuczna inteligencja zagrozi pozycji lekarza-diagnosty?
Odpowiedzi w programie #ObliczaMedycyny
#diagnostyka #kardiologia #ZdrowieCyfrowe #ZdrowieMobilne #EKG
Apple Heart Study: wykrywanie arytmii za pomocą Apple Watch.
Opublikowane: 6 grudnia 2017 Filed under: Choroby, Układ krążenia | Tags: Apple, Apple Watch, Badania kliniczne, dla pacjenta, Heart Study, mHealth, migotanie przedsionków, monitorowanie Dodaj komentarzApple Heart Study to pierwsze otwarte badanie kliniczne poświęcony wykrywaniu arytmii do którego dołączyć może praktycznie każdy użytkownik Apple Watch. Projekt prowadzony jest przez Uniwersytet Stanford i Apple. Celem badania jest ocena skuteczności wykrywania arytmii w ogólnej populacji osób poprzez automatyczne monitorowanie tętna wbudowanym w zegarku czujnikiem. Badanie jest nieinwazyjne i nie wymaga dodatkowego sprzętu, w tym klasycznego urządzenia EKG.
 Jak przebiega badanie?
Jak przebiega badanie?
W trakcie badania uczestnicy będą mieli automatycznie wykonywaną analizę czynności serca. W tym czasie wystarczy mieć założony zegarek na rękę. Osoby, u których zostanie zidentyfikowany rytm odpowiadający migotaniu przedsionków – najczęstszej nadkomorowej arytmii serca grożącej udarowi mózgu – otrzymają powiadomienie, oraz otrzymają bezpłatną poradę lekarską wraz z przyklejanym EKG do potwierdzenia wykrytej arytmii.
W jaki sposób zegarek wykrywa arytmię?
Tradycyjnym sposobem oceny rytmu serca, a więc i wykrywania arytmii (czynności niemiarowej), jest wykonanie zapisu EKG opartego na pomiarze różnicy potencjałów elektorycznych sczytywanych z klatki piersiowej i kończyn. W zegarkach Apple wykorzystywana jest jednak metoda oceny fali tętna za pomocą światła z diody LED i fotoczujnika. Wiemy, że kształt oraz miarowość tej fali koreluje z czynnością elektryczną serca, a zatem również z ewentualną arytmią.
Czy ten pomiar tętna jest prezycyjny?
Badania pokazują, że ocena fali tętna cechuje się mniejszą wartością diagnostyczną niż zapis EKG. Jednak z uwagi na powszechność i łatwość monitorowania pulsometr pozwala na zebranie większej ilości danych a tym samym zwiększa szansę na wykrycie arytmii.
Jak mogę wziąć udział w badaniu?
Aby wejść do badania należy pobrać aplikację Heart Study, mieć min. 22 lata, wyrazić zgodę na przetwarzanie danych i udział w badaniu oraz posiadać zegarek Apple Watch Series 1 lub wyższy. Uwaga posiadacze Apple Watch (1st generation) niestety nie będą mogli uczestniczyć w badaniu.
Skąd pobrać aplikację Heart Study?
Aplikacja jest dostępna pod linkiem: https://itunes.apple.com/us/app/apple-heart-study/id1277240928?mt=8 (wyłącznie amerykański AppStore)

Interpretacja EKG: lekarz kardiolog vs. sztuczna inteligencja
Opublikowane: 8 października 2017 Filed under: Badania kliniczne, Choroby, Układ krążenia | Tags: AI, ecg, Kardia, sieci neuronowe, szutczna inteligencja Dodaj komentarzOd kilku lat obserwujemy bardzo intensywny rozwój systemów wykorzystujących metody sztucznej inteligencji do interpretowania EKG i rozpoznawania istotnych klinicznie arytmii serca. Mimo, że dla większości praktykujących lekarzy, w tym kardiologów, zastąpienie doświadczonego oka algorytmem nadal jest pieśnią przyszłości, ostatnie pozytywne opienie Amerykańskiej Agencji ds. Leków (FDA, ang. Food and Drug Agency) dość istotnie skracają drogę do praktycznego wdrożenia takich rozwiązań.

Flagowym przykładem jest jednoodprowadzeniowe EKG Kardia, które może być umieszczone obudowie smartfona. Poza klasycznym zapisem czynności elektrycznej serca aplikacja zarządzająca urządzeniem posiada algorytm automatycznego rozpoznawania migotania przedsionków. To najczęstszy rodzaj arytmii, który nieleczony prowadzi do udaru niedokrwiennego mózgu oraz nasila niewydolność serca. W formie napadowej, migotanie przedsionków często sprawia trudność diagnostyczną i je zbyt późno rozpoznawane. Automatyzacja procesu i wyręczenie lekarza możnie mieć piramidalne ważne konsekwencji poprawy diagnostyki pacjentów i redukcji powikłań arytmii.
Opublikowane na łamach Circulation badanie REHEARSE-AF potwierdziło 4-krotnie większą częstość rozpoznania migotania przedsionków w grupie pacjentów stosujących EKG podłączone do smartfona dwa razy w tygodniu.

Przykładem projektu badawczego, który przekształcił się w funkcjonującą i certyfikowaną platformę do diagnostyki EKG jest francuski Cardiologs, który pozwala na automatyczną diagnostykę 10 arytmii, w tym również migotania przedsionków. Badania kliniczne wspierające technologią pokazują 91% dodatnią wartość predykcyjną i 97% czułość w wykrywaniu migotania przedsionków. Podobnie technologia iRhythm, również oparta na algorytmach sztucznej inteligencji, w badaniu walidującym koncepcję rozwiązania, w przypadku 14 z analizowanych 16 typów arytmii okazała się być skuteczniejsza od opisujących zapisy specjalistów kardiologii. Pojawia się zatem pytanie czy sięganie po tego typu rozwiązania to tylko oszczędność czasu lekarzy i redukcja kosztów, czy też może powinniśmy oceniać je również pod kątem bezpieczeństwa opieki medycznej.

Obok sygnału EKG równie atrakcyjną metodą detekcji arytmii jest analiza fali tętna monitorowanej za pośrednictwem pulsometrów umieszczonych w smartwatchach i opaskach monitorujących aktywność fizyczną. Ogłoszone w trakcie 38 konferencji Heart Rythem Society badanie mRhythm Study potwierdziło, że automatyczna analiza fali tętna wykonywana przez Apple Watch pozwala z 97% dokładnością wykryć migotanie przedsionków (ta funkcja nie jest jeszcze standardowo dostępna w oprogramowaniu watchOS). Warto zauważyć, że takie podejście nie wymaga od chorego żadnych dodatkowych czynności, poza założeniem rano zegarka na rękę.

Podsumowując, wprowadzenie technik opartych na metodach sztucznej inteligencji do budowania algorytmów interpretujących zapisy EKG pozwoliły na uzyskanie wyników porównywalnych lub lepszych od tradycyjnego podejścia. Najbliższe 12 miesięcy pokaże na ile szybko wyniki tych badań uda się wprowadzić do praktyki klinicznej, a aplikacje diagnozujące arytmie instalowane będą na telefonach i smartwatchach naszych pacjentów.
CoaguChek INRange – lepsza kontrola INR
Opublikowane: 24 października 2016 Filed under: Choroby, Układ krążenia | Tags: INR, krzepliwość, nowe leki przeciwzakrzepowe, PT Dodaj komentarzPolska przoduje w europejskim niechlubnym rankingu odsetka mieszkańców umierających z powodu udaru mózgu. W pierwszym miesiącu po udarze życie traci 40 proc. chorych, a po roku – 60 proc., czyli dwukrotnie więcej niż w Europie Zachodniej i USA. Aż 70 proc. tych, którzy przeżyją, zostaje inwalidami. Te niepokojące statystyki może zmienić upowszechnienie profilaktyki i leczenia przeciwzakrzepowego.
Przewlekłe choroby zwiększające ryzyko powstawania skrzeplin trzeba leczyć niekiedy do końca życia. Głównymi wskazaniami do przewlekłego leczenia przeciwzakrzepowego są choroby serca, a jednym z najczęstszych schorzeń stwarzających ryzyko powstawania zakrzepów, a więc także zawału mięśnia sercowego czy udaru mózgu, jest przetrwałe lub napadowe migotanie przedsionków.
Przy stosowaniu doustnego leczenia przeciwzakrzepowego niezbędne jest regularne kontrolowanie czasu protrombinowego u pacjentów i współczynnika INR (International Normalized Ratio). Przypomnijmy, że im wyższy wskaźnik INR, tym mniejsza krzepliwość krwi, a jego wartość w przypadku leczenia przeciwzakrzepowego zaleca się utrzymywać w przedziale 2,0-3,0.
Wizyty w laboratorium są jednak uciążliwe dla pacjentów, więc nic dziwnego, że dużą popularnością cieszą się aparaty do mierzenia INR w domu. Badania wskazują też, że pacjenci, którzy mają lepszy kontakt ze swoimi lekarzami, lepiej stosują zasady konieczne, aby terapia przeciwzakrzepowa nie tylko była skuteczna, ale i bezpieczna. Firma Roche wprowadziła właśnie na europejski rynek CoaguChek INRange, pierwszy system do domowego oznaczania INR wyposażony w technologię Bleutooth, dzięki której lekarze mogą na bieżąco monitorować terapię. Urządzenie, tak jak poprzednie modele CoaguChek, działa podobnie jak glukometr. Do przeprowadzenia badania wystarczy kropla krwi kapilarnej pobranej w domu chorego przez niego samego z opuszka palca i zaledwie minuta, by uzyskać precyzyjny wynik, który równocześnie trafia bezpośrednio do kliniki. Jednocześnie pacjent otrzymuje informację, czy wynik mieści się w granicach wyznaczonych przez lekarza, czy też odbiega od normy. Odczytanie informacji ułatwia choremu kolorowy wyświetlacz. Dodatkowo użytkownik urządzenia przy każdym wyniku może dodać sześć notatek o tym, co działo się przed pomiarem, a mogło mieć wpływ na jego wynik. Można też zaprogramować alarmy informujące o zbliżającej się porze pomiaru krzepliwości, zażycia leków czy terminie wizyty u lekarza.
Materiał graficzny: Roche
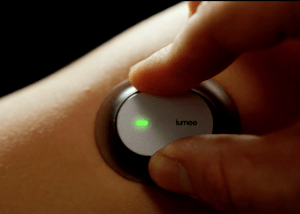
Lumee Oxygen Sensing System – wszczepialny czujnik do określania utlenowania tkanek
Opublikowane: 10 października 2016 Filed under: Cukrzyca, Układ krążenia, Układ oddechowy | Tags: bezdech senny, choroby tętnic obwodowych, Cukrzyca, PAD, POChP Dodaj komentarzKiedy w styczniu na targach CES 2016 przedstawiciele firmy Profusa zaprezentowali prototyp wszczepianego pod skórę czujnika Lumee, służącego do określania stężenia różnych substancji w organizmie, spotkali się z bardzo dużym zainteresowaniem. Nic dziwnego, wiele wskazuje na to, że już niebawem urządzenia wszczepialne mogą zająć na rynku mocną pozycję obok bardzo popularnych obecnie urządzeń ubieralnych (ang. wearables), zwłaszcza w przypadku osób cierpiących na wymagające ciągłego monitorowania choroby przewlekłe.
Twórcy z Profusa nie ukrywają, że chociaż na razie nie udało im się osiągnąć głównego celu, czyli opracować czujnika służącego do określania stężenia glukozy w organizmie, to są zadowoleni ze swojego pierwszego produktu, Lumee Oxygen Sensing System, który obecnie czeka na akcept ze strony Amerykańskiej Agencji ds. Żywności i Leków – FDA i przyznanie znaku CE (w Europie ma być dostępny jeszcze w tym roku).
Lumee Oxygen Sensing System, czujnik służący do ciągłego określania utlenowania znajdujących się obok niego tkanek, ma być wykorzystywany przede wszystkim do monitorowania gojenia się ran, np. u osób z przewlekłymi owrzodzeniami żylnymi czy chorujących na cukrzycę. Czujnik przeznaczony jest także dla osób cierpiących na choroby tętnic obwodowych (peripheral artery disease, PAD).
Szacuje się, że PAD występuje u 202 milionów ludzi na świecie, w tym u 27 milionów w Europie i Ameryce Północnej. Jest to grupa chorób, których najczęstszą przyczyną jest miażdżyca i które przebiegają ze zwężeniem lub niedrożnością tętnic obwodowych, co w konsekwencji powoduje niedokrwienie kończyn dolnych. PAD na początku często przebiegają bezobjawowo (tylko u 10-15% chorych stwierdza się ból nóg podczas chodzenia, czyli chromanie przestankowe; innymi objawami mogą być marznięcie stóp, zaniki mięśniowe, zaniki owłosienia, trudno gojące się rany lub owrzodzenia). Chorzy narażeni są na wystąpienie zgorzeli (co może doprowadzić nawet do amputacji), należą także do grupy osób o zwiększonym ryzyku zgonu z powodu zawału mięśnia sercowego i udaru.
To, co może być pomocne w prowadzeniu leczenia PAD, to kontrola utlenienia tkanek zajętej kończyny. Jest to niezwykle istotne w procesie gojenia się ran, a także może uchronić pacjenta przed pogorszeniem się sprawności ruchowej czy rozwinięciem się zgorzeli.
Takie zadanie ma przed sobą Lumee Oxygen Sensing System. Lumee zbudowany jest z maleńkich bioczujników (3-5 mm), które umieszczane są pod skórą za pomocą igły, oraz czytnika optycznego.
Bioczujniki osadzone są na specjalnym hydrożelu, który przypomina materiał, z jakiego zrobione są soczewki kontaktowe, i nie wywołuje reakcji odrzucenia przez organizm. Hydrożel jest połączony z molekułą, która emituje fluorescencyjne światło zmieniające się w zależności od poziomu utlenowania tkanki. Czujnik optyczny, umieszczany na skórze, odczytuje sygnał fluorescencyjny i wysyła dane do smartfona. Co ważne, bioczujniki działają aż do dwóch lat i po tym czasie nie trzeba ich usuwać z organizmu.
Lumee jest urządzeniem, który ma duży potencjał nie tylko w opiece medycznej, ale również w obszarze badań klinicznych, a nawet wellness czy fitness. Jego twórcy pracują też nad dostosowaniem go do określania stężenia w organizmie innych substancji, takich jak kreatynina czy glukoza. Myślą również o wykorzystaniu urządzenia w monitorowaniu takich chorób, jak przewlekła obturacyjna choroba płuc (POChP) czy bezdech senny (OBS)
Materiały graficzne: Profusa
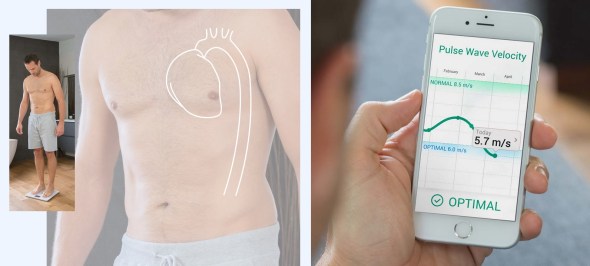
Body Cardio – waga mierząca prędkość fali tętna
Opublikowane: 7 października 2016 Filed under: Choroby, Cukrzyca, Układ krążenia | Tags: BMI, prędkość fali tętna, PWV, waga Dodaj komentarzPierwszy raz o bezprzewodowej wadze francuskiej firmy Withings pisaliśmy już w 2012 roku. Jej twórcy cały czas pracowali nad udoskonaleniem produktu, dzięki czemu na rynek trafiła właśnie najbardziej zaawansowana na świecie waga – Body Cardio. Oczywiście nie zaskakuje informacja, że waga pokazuje, ile ważymy, jakie jest nasze BMI oraz w jakim procencie nasz organizm składa się z tłuszczu, mięśni i wody. Nie dziwi także to, że waga wyświetla, jaki jest rytm naszego serca, a nawet to, jaka jest pogoda i temperatura na zewnątrz, a także synchronizuje się z urządzeniem do pomiaru aktywności, czy łączy bezprzewodowo ze smartfonem (dane wyświetlane są w aplikacji Health Mate: iOS, Android).
Tym, co wyróżnia Body Cardio od innych produktów tego typu, jest to, że mierzy ona także prędkość fali tętna (Pulse Wave Velocity, PWV). PWV, wskazująca na stopień elastyczności/sztywności dużych naczyń tętniczych, uznana jest za ważny parametr oceny ryzyka chorób układu krążenia i według wytycznych ESH/ESC jej określenie należy do badań zalecanych u chorych na nadciśnienie tętnicze.
Wartości PWV rosną wraz w wiekiem i są tym większe, im sztywniejsze są naczynia: u dzieci wynoszą 5–6 m/s, u osób w wieku 20–50: 7–9 m/s, a u osób po 50. roku życia do 12 m/s (uważa się, że jeśli PWV wynosi powyżej 12 m/s, to u pacjenta występują już zmiany w narządach wewnętrznych spowodowane nadciśnieniem tętniczym). Nieprawidłową PWV stwierdza się u osób starszych, z nadciśnieniem, hipercholesterolemią, cukrzycą typu 2 czy przewlekłą niewydolnością nerek, i świadczy ona o zwiększonym ryzyku zgonu z dowolnej przyczyny oraz z przyczyn sercowo-naczyniowych w tej grupie chorych. Co więcej, wskazuje także na zwiększone ryzyko wystąpienia choroby niedokrwiennej serca oraz udaru mózgu u osób zdrowych.
Za złoty standard w badaniach sztywności ściany aorty uważany jest pomiar PWV pomiędzy tętnicami szyjną i udową, i najczęściej przeprowadzany jest przy użyciu tonometru aplanacyjnego (rekonstrukcja fali ciśnienia aortalnego na podstawie fali tętna zarejestrowanej na obwodzie).
Waga Body Cardio ocenia PWV, obliczając czas przejścia fali tętna (Pulse Transit Time), czyli czas między wyrzutem krwi z aorty a dotarciem jej do stóp. Chociaż jej twórcy podkreślają, że nie jest to urządzenie medyczne, zlecili jednak przeprowadzenie badania oceniającego u 111 pacjentów dokładność pomiarów PWV przez wagę w porównaniu z aparatem wykorzystującym tonometrię aplanacyjną. Wyniki wskazały na porównywalną dokładność oznaczeń.
Materiały graficzne: Withings